公開日 2014/06/25
更新日 2021/12/17
【化学講師向け】高校化学・電池の仕組み!!~電池の反応式~

[電池の仕組み]高校化学・すっきり教える電池の仕組み!!
も参照してくださいね!
電池の反応
日常で使われる電池はマンガン乾電池が多いのですが、
大学入試で良く問われるボルタ電池・ダニエル電池を確認します!!


ボルタ電池では、起電力が最初約1.1Vであるが最後は0.4V位まで下がってしまいます。
→この現象を分極と呼びます。

【ボルタ電池とダニエル電池の違い】
・ボルタ電池:水素ガスの気泡が反応を阻害
・ダニエル電池:銅が析出するので反応を阻害しない。充電可能
ダニエル電池の仕組み↓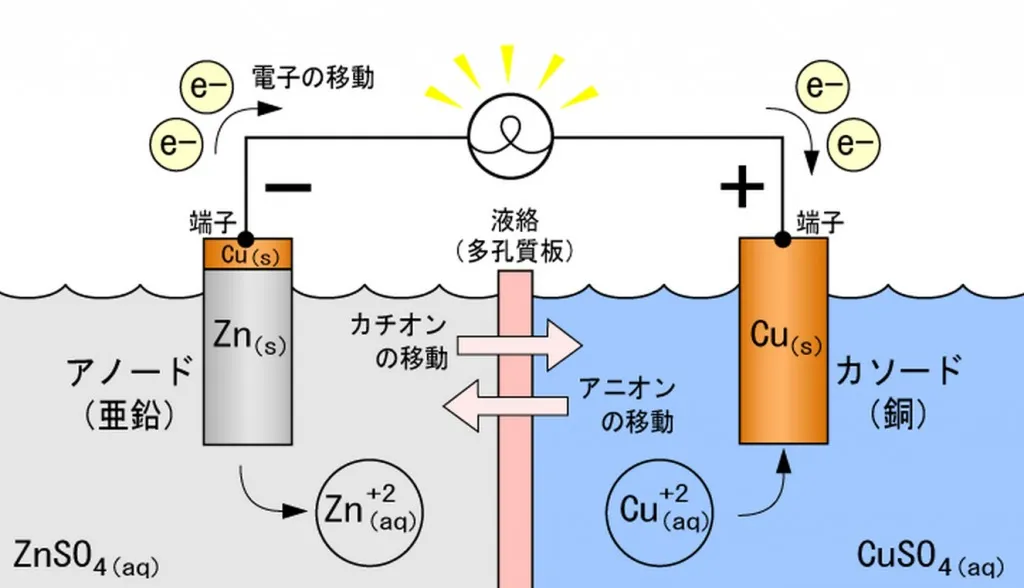
素焼き板を硫酸イオンが行き来できる。
硫酸イオンの正極側と負極側で濃度に差が生じ、これを均一にするために硫酸イオンは負極側へ移動。
正極側では硫酸イオンの移動により、プラスイオン(銅イオン)が余る。この銅イオンが電子を受け取る。
参考リンク:電池・電気分解


![10円玉をピカピカにしよう!![高校化学]](https://www.juku.st/cdn/article_images/304/large_juku_entry_images_image.webp)